| کد مقاله | کد نشریه | سال انتشار | مقاله انگلیسی | نسخه تمام متن |
|---|---|---|---|---|
| 5370822 | 1503910 | 2016 | 13 صفحه PDF | دانلود رایگان |
عنوان انگلیسی مقاله ISI
ALG-2 divalent-ion affinity: Calorimetric analysis of the des23 versions reveals high-affinity site for Mg2 +
دانلود مقاله + سفارش ترجمه
دانلود مقاله ISI انگلیسی
رایگان برای ایرانیان
کلمات کلیدی
ABMIPTGEGTAITCHBSHepes, 4-(2-hydroxyethyl)-1-piperazineethanesulfonic acid - Hepes، 4- (2-hydroxyethyl) -1-piperazineethanesulfonic acidEDTA - اتیلن دی آمین تترا استیک اسید Ethylenediaminetetraacetic acid - اتیلینیدامین تتراستیک اسیدisopropyl-β-d-thiogalactopyranoside - ایزوپروپیل-ب-دی-تیوگالکتوپیرانوزید
موضوعات مرتبط
مهندسی و علوم پایه
شیمی
شیمی تئوریک و عملی
پیش نمایش صفحه اول مقاله
چکیده انگلیسی
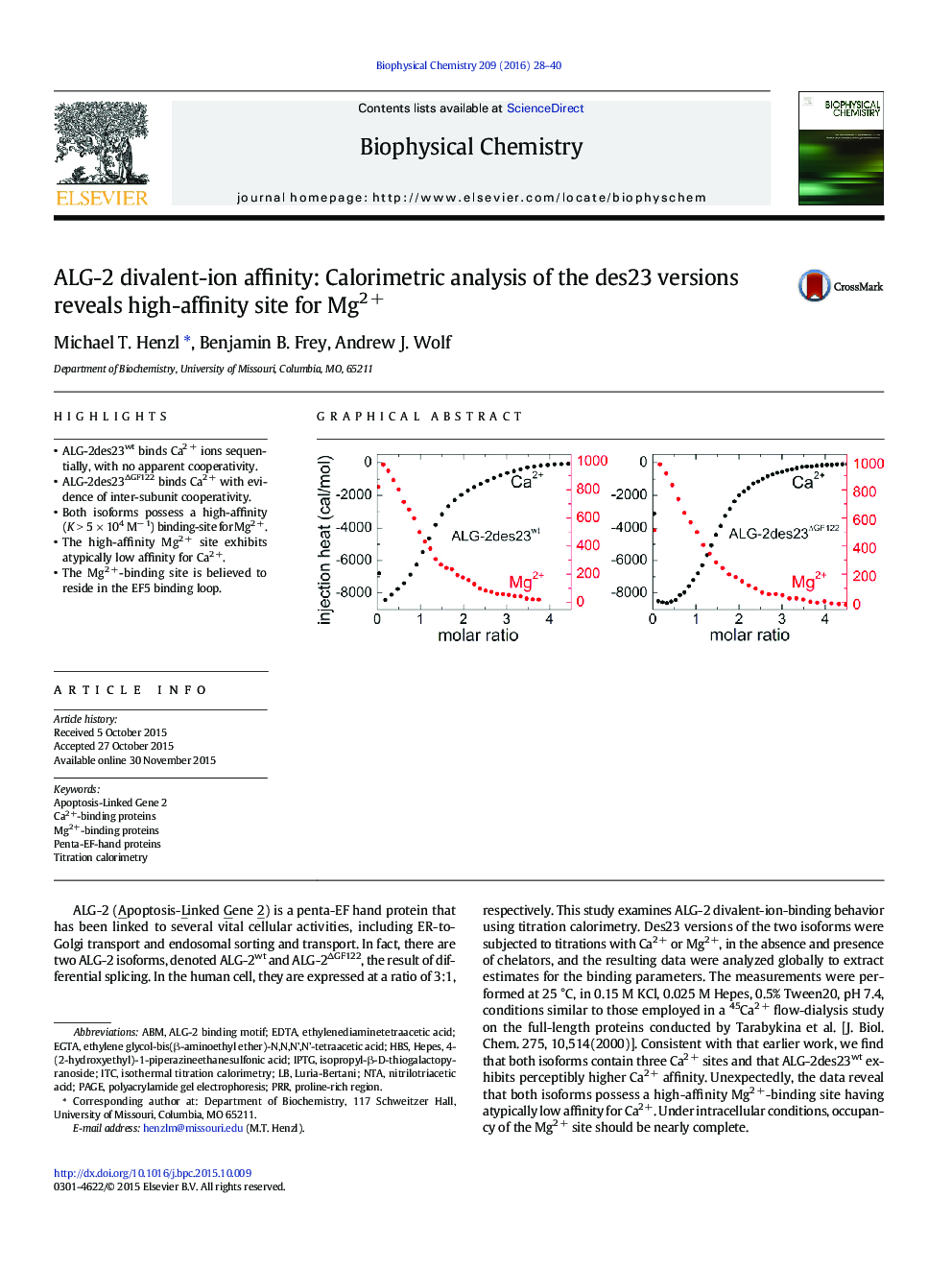
- ALG-2des23wt binds Ca2Â + ions sequentially, with no apparent cooperativity.
- ALG-2des23ÎGF122 binds Ca2Â + with evidence of inter-subunit cooperativity.
- Both isoforms possess a high-affinity (K > 5 Ã 104 Mâ 1) binding-site for Mg2 +.
- The high-affinity Mg2Â + site exhibits atypically low affinity for Ca2Â +.
- The Mg2Â +-binding site is believed to reside in the EF5 binding loop.
ناشر
Database: Elsevier - ScienceDirect (ساینس دایرکت)
Journal: Biophysical Chemistry - Volume 209, February 2016, Pages 28-40
Journal: Biophysical Chemistry - Volume 209, February 2016, Pages 28-40
نویسندگان
Michael T. Henzl, Benjamin B. Frey, Andrew J. Wolf,